生物学的製剤とバイオシミラーの違いをご存じですか?薬価の高い生物学的製剤も、特許切れ後にはバイオシミラーが登場し、医療費削減が期待されています。しかし、生物学的製剤は化学合成薬と異なる特殊な薬です。その管理には細心の注意が必要で、薬局で先発品をバイオシミラーに簡単に切り替えることもできません。本記事では、薬剤師が知るべき生物学的製剤とバイオシミラーの基礎知識から、調剤時の留意点や患者さんへの説明ポイントまで、わかりやすく解説します。
生物学的製剤とは何か?
生物学的製剤とは、細胞や微生物など生物の力を利用して作られる医薬品のことです。従来の医薬品(化学合成医薬品)は化学反応を起こして有効成分を合成します。一方、生物学的製剤は遺伝子組換え技術や細胞培養技術を駆使し、生きた細胞に有効なタンパク質を作らせて製造するという違いがあります。
例えばヒトのホルモンや酵素、抗体といったタンパク質を作り出し、それ自体を薬として利用します。分子量が大きく複雑な構造を持つタンパク質は化学的に合成することが難しいため、生物の力を借りる必要があるのです。
生物学的製剤の定義と特徴
生物学的製剤(生物学的製剤は「バイオ医薬品」とも呼ばれます)は、遺伝子組換えや培養技術を用いて生体由来のタンパク質を有効成分とする医薬品です。インスリンや抗体医薬品などが代表例で、低下した体内のインスリンを補充したり、特定の分子を狙って作用することで疾患を治療します。
その特徴として、標的分子に対する作用の精密さが挙げられます。例えば、抗体医薬品はがん細胞だけを攻撃し副作用を抑えることが期待できるなど、難治性疾患に対して画期的な効果をもたらしています。
ただし、生物由来である以上免疫反応(アレルギー等)が起こるリスクはゼロではなく、安全性確保のため製造過程や品質管理は非常に厳格に行われています。
生物学的製剤の代表例と役割
代表的な生物学的製剤には、糖尿病治療に使われるインスリン製剤、関節リウマチや炎症性腸疾患の治療に使われる抗体医薬品(例:抗TNFα抗体)、特定の酵素が欠乏する疾患に補充する酵素製剤などがあります。これら生物学的製剤は、それまで治療が難しかった病気に新たな治療法を提供し、多くの患者さんのQOL向上に貢献しています。一方で製造コストが高く、冷蔵保存が必要など管理も難しいため、薬価が高額になりがちです。そのため、医療現場では費用対効果や適正使用を考慮しながら、生物学的製剤を必要な患者さんに適切に提供することが求められています。
バイオシミラーとは何か?
バイオシミラーとは、先行する生物学的製剤(先発品)の特許が切れた後に、別のメーカーから発売される後発の生物学的製剤です。化学合成薬でいう「ジェネリック医薬品」に相当しますが、後述するようにジェネリックとは承認の扱いが異なります。
バイオシミラーは先発品と有効成分(例えばインスリンならインスリンそのもの)のアミノ酸配列は同一で、効能・効果や用法用量も基本的に同じです。
ただし、生物を用いて製造する関係上、先発品と完全に同じ製品を再現することはできないため「シミラー(similar=類似)」と呼ばれます。つまり、バイオシミラーは先発品と極めて高い類似性を持ち、品質特性に多少の差異があっても安全性・有効性に影響しないことが確認された医薬品です。
バイオシミラーの定義と特性
バイオシミラーは品質・安全性・有効性が先行バイオ医薬品と同等・同質であることが証明された医薬品です。価格は、国のルールにより先行品の原則70%程度の薬価に設定されます。このように経済的メリットが大きい点がバイオシミラーの特性ですが、同時に「全く同じものではない」という点に注意が必要です。
バイオシミラーの名称には一般に成分名+「BS」(BioSimilarの略)といった表記がなされ、医療現場で区別できるようになっています。薬剤師は先発品とバイオシミラーの外観が類似している場合もあるため、処方箋記載の名称をしっかり確認する必要があります。
バイオシミラーの承認プロセスと価格
バイオシミラーの承認には、新薬に準じた厳格な審査が行われます。従来のジェネリック医薬品の場合、先発品と有効成分の同一性の確認と、生物学的同等性試験により承認可能です。
一方バイオシミラーでは、先発品との品質特性の詳細な比較試験、品質・非臨床試験による比較、さらに臨床試験(比較試験)によって効果と安全性が同等であることを示す必要があります。開発コストは新薬ほどではないものの、ジェネリックよりは大幅にかかるため、価格もジェネリックほど安くはなりません。
日本では薬価制度上、先発品に対し原則7割の価格設定ですが、開発段階の臨床試験充実度に応じて最大+10%の加算が認められる仕組みがあります。医療費削減のため、政府はバイオシミラーの使用促進に向けて具体的な数値目標を設定し、その普及を後押ししています。薬剤師としても、バイオシミラーの適切な活用が今後さらに求められるでしょう。
ジェネリック医薬品とバイオシミラーの違い
前述のとおり、バイオシミラーは「生物学的製剤版の後発医薬品」ですが、通常の後発医薬品(ジェネリック医薬品)とは異なる点が多々あります。ジェネリック医薬品は先発医薬品と同じ有効成分・剤形であれば基本的に同じもの(同一品質)とみなされますが、バイオシミラーは「同等・同質」ではあっても「同一」ではありません。
ここではジェネリックとバイオシミラーの製造面・品質面および制度面での違いを整理します。薬剤師が現場で先発品・ジェネリック・バイオシミラーを扱う際に混同しないよう、それぞれの特徴を正しく理解しておきましょう。
成分・製造方法と品質評価の違い
ジェネリック医薬品は、先発医薬品と同じ有効成分を含み、錠剤やカプセルなど投与経路が同一であることが前提です。添加物が一部異なる場合はありますが、近年では先発と添加物まで同じ「オーソライズド・ジェネリック」も登場しています。有効成分がまったく同じで製法も化学合成で再現性が高いため、品質は理論上先発品と同一といえます。
これに対しバイオシミラーは、先行バイオ医薬品とアミノ酸配列は同じですが、製造に使う細胞株や培養条件が異なるため、分子にわずかな違い(例:糖鎖の構造の違いなど)が生じる可能性があります。そのため、承認前の審査項目も増え、製造後の各ロットごとの品質試験も非常に厳密です。いずれも患者さんに安全で有効な薬を届けるための工夫ですが、バイオシミラーはジェネリック以上に品質管理が重視されている点を理解しておきましょう。
製造販売後調査の違いについて
製造販売後調査の違い: ジェネリック医薬品では、特段の理由がない限り製造販売後調査は義務付けられていません。これに対しバイオシミラーは、先発品と極力同等に作られているとはいえ生物由来製剤特有のリスク(免疫原性など)が残る可能性があります。そのため、バイオシミラーの製造販売業者には、製造販売後調査が義務づけられているのです。
具体的には、医薬品リスク管理計画(RMP)を策定し、安全性について継続的にモニタリングをすることになっています。
ここまで紹介したジェネリック医薬品とバイオシミラーの違いを表にまとめました。
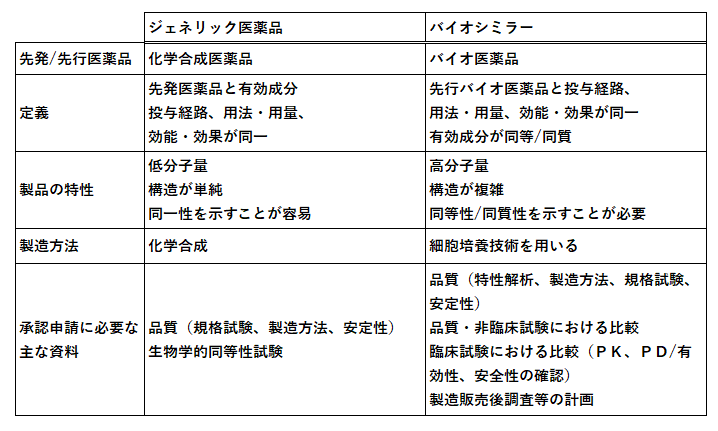
参考:バイオ医薬品・バイオシミラーを正しく理解していただくために 平成31年2月厚生労働省医政局経済課
医薬品医療機器総合機構:バイオシミラーの規制について
薬局でバイオシミラーへ変更調剤は可能?
調剤現場の薬剤師が特に気になるのが、「処方せんの先発医薬品を薬局でバイオシミラーに置き換えてよいか」という点でしょう。ジェネリック医薬品であれば、処方せんに「変更不可」の指示がなければ薬剤師の判断で先発品から後発品へ変更調剤できます。しかし、バイオシミラーの場合、薬剤師の判断での変更は認められていません。ここでは、その理由について解説します。
処方箋上の扱い:バイオシミラーは銘柄指定
日本の調剤制度では、ジェネリック医薬品の普及を促進するため、処方医が先発品名で処方していても「変更不可」にチェック等がなければ薬剤師判断で後発品に差し替え可能というルールがあります。
しかしバイオシミラーはこのルールの対象外です。厚生労働省は現時点で「薬剤師の判断で生物学的製剤を別の製剤に自動的に切り替えることは推奨しない」と明言しています。そのため、バイオシミラーを使用したい場合には医師が処方箋にそのバイオシミラーの銘柄を書かなければならないという運用になっています。
具体例を挙げれば、医師がインスリン製剤「ランタス注ソロスター(先行品)」と処方箋に記載した場合、薬剤師は勝手に「インスリングラルギンBS注○○」(バイオシミラー)に置き換えて調剤することはできません。同様に、医師があるバイオシミラー製品を処方した場合に、それを別メーカーのバイオシミラーに変更するといったことも認められていません。
要するに、生物学的製剤(先発品)およびそのバイオシミラーは、処方箋上は一つひとつ別個の医薬品として扱われており、薬局での代替調剤は制度上許されていないのです。
なぜ薬剤師による代替不可なのか
なぜバイオシミラーは薬剤師の判断でジェネリックのように代替できないのでしょうか。その背景には、これまで述べてきたバイオシミラーの特性があります。すなわち、生物学的製剤は極めて複雑で、先発品とバイオシミラーが完全に同一ではないためです。わずかな違いであっても、患者さんによって副作用の出方や体の反応に差が生じる可能性があるため、処方医の判断を経ずに別の製剤へ切り替えるのは、安全管理の面から好ましくないとされています。薬剤師は患者さんから相談を受けた場合も、このルールを踏まえて適切に対応しなければなりません。
まとめ
生物学的製剤とバイオシミラーの違い、および薬局での取り扱いポイントについて解説しました。
生物学的製剤は生きた細胞を使って作られる特殊な医薬品であり、画期的な治療効果を持つ反面、管理に注意が必要です。一方のバイオシミラーはその先発品に極めて近い後発医薬品で、効果や安全性は同等でありながら医療費の節減に寄与します。
しかし、バイオシミラーはジェネリック医薬品とは承認制度や品質管理が異なり、薬剤師の判断で先発品と置き換えることはできません。薬局での変更には必ず医師の指示が必要となります。
薬剤師として、まず両者の定義や特徴を正しく理解することが重要です。バイオシミラーがなぜ“同じ”ではなく“類似”なのかを知ることで、日々の調剤や患者対応にも説得力が増します。さらに、経済性と治療効果のバランスを考慮する視点も大切です。薬剤師は先発品とバイオシミラーそれぞれのメリットを踏まえ、患者さんや医師と相談しながら最適な選択肢を提示できると理想的です。例えば患者さんから費用の相談を受けたら、医師にバイオシミラーへの変更を提案することも必要となってきます。もちろん最終的な処方判断は医師に委ねられますが、医師との連携によって患者さん主体の治療を実現する架け橋となるのも、これからの薬剤師の重要な役割でしょう。
参考:厚生労働省バイオ医薬品とはmhlw.go.jp
厚生労働省 後発医薬品(ジェネリック医薬品)及びバイオ後続品(バイオシミラー)の使用促進について
厚生労働省医政局経済課 バイオ医薬品・バイオシミラーを 正しく理解していただくために
一般社団法人日本バイオシミラー協議会 バイオシミラーが患者さんと社会にもたらすメリットとは?
厚生労働省 ジェネリック医薬品の生物学的 同等性についての考え方









